

守正中西・创新治血丨学术讲坛・第1期——《再生障碍性贫血研
快速问专家,今日还剩下16个专家号
免费拨打
免费咨询
“守正中西”——坚守中医整体辨证与西医精准诊疗的双重根基;
“创新治血”——以临床需求为导向,融合前沿科技,不断优化血液病诊疗策略。
《学术讲坛》是济南血液病医院倾力打造的高端学术交流平台,由「享国务院特殊津贴专家」葛林阜院长领衔主讲,定期围绕血液病领域年度国际进展、指南更新、临床难点及本院实践经验等进行系统分享。内容面向临床医生及患者家属,旨在传递循证、启发思考、促进共进。本期为第1期,聚焦再生障碍性贫血(AA)。葛院长结合第67届美国血液学会(ASH)年会最新发布的重磅研究,从疾病机制、造血干细胞移植、TPO-RA联合免疫抑制治疗、新型靶向疗法四大维度,为全院医生带来前沿解读。以下为精华整理。


 一、机制研究新突破:解码克隆演变
一、机制研究新突破:解码克隆演变
AA是一种T细胞攻击造血干祖细胞(HSPCs)导致的骨髓衰竭性疾病。当前临床面临的核心痛点包括:诊断缺乏生物标志物、传统分型方式过时、免疫抑制治疗(IST)应答率有限(约30%-40%无应答),且部分患者会进展为髓系恶性肿瘤。
来自英国学者的研究(2025 ASH Oral 25)通过对AA和PNH患者进行全基因组测序和全外显子双工测序,揭示了疾病体细胞演化的全新图景。研究发现:
免疫逃逸突变出现极早:
部分患者的关键突变在受孕后10周内就已经发生,早于临床诊断数年至数十年;
PNH克隆潜伏期超长:
优势PIGA突变多发生在生命首个十年,距临床发病潜伏期长达30-40年;
新发现受选择基因:
ERAP2和RUNX1T1被鉴定为新的驱动基因,为机制研究和治疗靶点开发提供了新方向。
这一发现对于临床的启示意义重大——通过克隆结构分析,有望将患者区分为“免疫逃逸主导型”和“髓系驱动基因主导型”,从而指导个体化治疗选择,避免无效的免疫抑制治疗,并对恶性转化高危患者实现早期识别与干预。
二、移植治疗新进展:方案优化升级
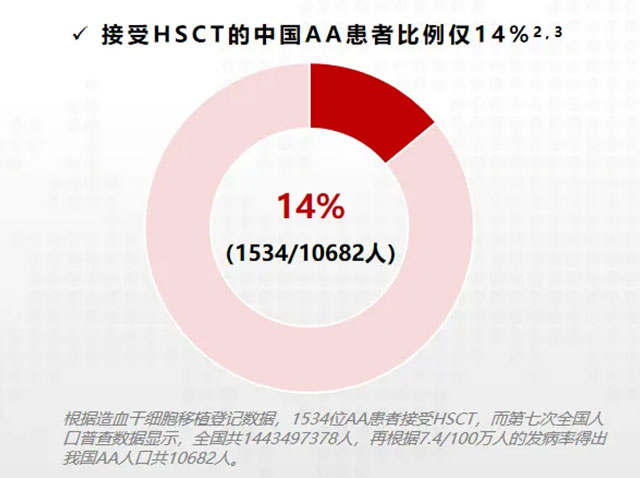 造血干细胞移植(HSCT)仍是治愈AA最彻底的手段,但供者来源、医疗资源和经济成本限制了其可及性。根据国内数据,接受HSCT的中国AA患者比例仅约14%。本次ASH年会公布了多项移植领域的重要突破。
造血干细胞移植(HSCT)仍是治愈AA最彻底的手段,但供者来源、医疗资源和经济成本限制了其可及性。根据国内数据,接受HSCT的中国AA患者比例仅约14%。本次ASH年会公布了多项移植领域的重要突破。
阿仑单抗预处理方案:10年OS优异
英国33个中心的大规模回顾性研究(2025 ASH Oral 984)纳入了1999-2024年间所有接受HLA 9-10/10同胞或无关供体移植的SAA和遗传性骨髓衰竭综合征患者,共涵盖数百例移植病例。结果显示:以阿仑单抗为基础的FCC方案(氟达拉滨+环磷酰胺+阿仑单抗)预处理的10年总生存率达85%,10年无GVHD无复发生存率为85%。其中,儿童患者10年OS高达94%。骨髓作为干细胞来源在儿童患者中优势尤为显著(OS 95%vs外周血88%,P=0.01)。年龄越小、使用FCC方案、身体状况越好的患者,预后越佳。
Omidubicel扩增脐带血移植:总生存率94%
对于缺乏HLA匹配供体的难治性SAA患者,一项II期临床研究(2025 ASH Poster 5963)探索了Omidubicel——一种体外烟酰胺扩增脐带血移植方案。研究共纳入18例对IST治疗无效的SAA患者,中位年龄19岁。结果令人振奋:94%的患者实现中性粒细胞恢复(中位8天),89%实现血小板恢复(中位24天),94%达到完全髓系嵌合。无III-IV级急性GVHD或慢性GVHD发生,总生存率达94%。这一方案为无合适供体的高危AA患者提供了可行的替代移植来源。
三、TPO-RA联合IST:一线治疗地位持续巩固
移植虽好,但多数患者仍依靠药物治疗。目前,TPO-RA联合IST已被国内外指南确立为不适合移植SAA患者的一线标准治疗方案。
艾曲泊帕:尽早启动安全可行
一项前瞻性II期研究(2025 ASH Oral 979)评估了在等待确诊检查和启动正式治疗期间,尽早启动低剂量环孢素联合艾曲泊帕方案的安全性与可行性。结果显示:该方案安全可行,无治疗相关严重不良事件,且中性粒细胞计数在hATG治疗前即显著改善。2年复发率(16%vs32%)和高危克隆演进率(3%vs13%)均呈下降趋势,提示尽早干预可能减少骨髓应激造血相关的克隆异常。
海曲泊帕:老年患者疗效更优
北京大学血液病研究所开展的单中心回顾性研究(2025 ASH Poster 1119)纳入了32例年龄≥60岁的SAA或VSAA患者,比较了海曲泊帕联合IST与单纯IST的疗效。结果显示:12个月累积缓解率分别为92.9%和85.7%,完全缓解率分别为35.7%和33.3%。12个月总生存率为83.3%。在Charlson合并症指数更高、粒细胞缺乏更严重的情况下,海曲泊帕联合组仍展现了更优的疗效,且耐受性良好。
2025年专家共识:TPO-RA推荐力度加强
2025年1月,中华医学会血液学分会红细胞疾病学组正式发布《促血小板生成药物治疗再生障碍性贫血专家共识》,对艾曲泊帕、海曲泊帕、罗普司亭等药物的临床应用作出了更明确的推荐,并对SAA、NSAA、TD-NSAA等不同患者类型提供了差异化的治疗路径。共识还特别强调了特殊人群(儿童、孕产妇、老年人、肝功能异常者)的个体化用药策略。
四、新型疗法探索
除了上述成熟的治疗策略,本次ASH年会还公布了多项探索性疗法的研究成果。
IL2RG抗体(REGN7257):首次人体研究展现安全性
REGN7257是一种能阻断IL2RG的单克隆抗体。γ链细胞因子(包括IL2、IL4、IL7、IL9、IL15、IL21)在T细胞发育和激活中起关键作用,阻断其共同受体亚基有望成为抑制致病性T细胞反应的新策略。这项I期、多中心、首次人体研究纳入了17例既往IST治疗难治或复发的SAA患者。结果显示,REGN7257总体耐受性良好。1例IST复发患者在首次给药后即出现血液学反应,且重复给药后反应再次出现。该研究为IL2RG阻断剂在轻症SAA及其他T细胞介导疾病中的进一步探索奠定了基础。
罗特西普+CsA+艾曲泊帕三联疗法:抑制焦亡促进造血
天津医科大学总医院付蓉教授团队的研究(2025 ASH Poster 4976)发现,罗特西普能够通过抑制单核细胞中NF-κB/NLRP3信号轴,实现SAA的多靶点免疫调节。三联疗法显著恢复了SAA患者的造血功能,但停药后仍存在复发问题,提示长期维持治疗的必要性。单细胞RNA测序显示,复发期间单核细胞中焦亡相关基因表达升高。机制层面,罗特西普可显著降低单核细胞焦亡相关基因及促炎细胞因子表达,同时减弱CD8⁺T细胞的炎症因子分泌和细胞毒分子活性,从而破坏致病恶性循环,促进造血恢复。
芦可替尼:降低巨噬细胞焦亡治疗SAA
JAK1/2抑制剂芦可替尼(Ruxolitinib)在SAA治疗中的潜力也受到关注。体外及动物模型实验表明,芦可替尼可通过降低巨噬细胞焦亡水平,改善免疫微环境,并可能通过调控MHC II分子及JAK/STAT通路影响T细胞活化。此外,在仅接受外周血干细胞移植的AA患者中,围移植期加用芦可替尼作为GVHD预防药物,可显著降低II-IV级急性GVHD发生率,并改善患者无GVHD-无失败生存率。
葛林阜院长从机制到临床,AA精准诊疗未来可期
葛林阜院长在授课中强调,2025 ASH大会的研究成果从机制解码、移植优化、药物升级到创新探索,全面推动了AA诊疗的发展。当前AA治疗已形成“移植根治+药物兜底+创新补位”的多元格局,精准化、个体化成为核心趋势。

 对于患者而言,AA并非不治之症,随着诊疗技术的进步,无论是儿童、青年还是老年患者,都能找到适合的治疗方案,应保持信心并积极配合治疗;对于同领域医生,需紧跟学术前沿,将新进展、新方案融入临床实践,为患者提供更优质的诊疗服务。
对于患者而言,AA并非不治之症,随着诊疗技术的进步,无论是儿童、青年还是老年患者,都能找到适合的治疗方案,应保持信心并积极配合治疗;对于同领域医生,需紧跟学术前沿,将新进展、新方案融入临床实践,为患者提供更优质的诊疗服务。
“创新治血”——以临床需求为导向,融合前沿科技,不断优化血液病诊疗策略。
《学术讲坛》是济南血液病医院倾力打造的高端学术交流平台,由「享国务院特殊津贴专家」葛林阜院长领衔主讲,定期围绕血液病领域年度国际进展、指南更新、临床难点及本院实践经验等进行系统分享。内容面向临床医生及患者家属,旨在传递循证、启发思考、促进共进。本期为第1期,聚焦再生障碍性贫血(AA)。葛院长结合第67届美国血液学会(ASH)年会最新发布的重磅研究,从疾病机制、造血干细胞移植、TPO-RA联合免疫抑制治疗、新型靶向疗法四大维度,为全院医生带来前沿解读。以下为精华整理。



AA是一种T细胞攻击造血干祖细胞(HSPCs)导致的骨髓衰竭性疾病。当前临床面临的核心痛点包括:诊断缺乏生物标志物、传统分型方式过时、免疫抑制治疗(IST)应答率有限(约30%-40%无应答),且部分患者会进展为髓系恶性肿瘤。
来自英国学者的研究(2025 ASH Oral 25)通过对AA和PNH患者进行全基因组测序和全外显子双工测序,揭示了疾病体细胞演化的全新图景。研究发现:
免疫逃逸突变出现极早:
部分患者的关键突变在受孕后10周内就已经发生,早于临床诊断数年至数十年;
PNH克隆潜伏期超长:
优势PIGA突变多发生在生命首个十年,距临床发病潜伏期长达30-40年;
新发现受选择基因:
ERAP2和RUNX1T1被鉴定为新的驱动基因,为机制研究和治疗靶点开发提供了新方向。
这一发现对于临床的启示意义重大——通过克隆结构分析,有望将患者区分为“免疫逃逸主导型”和“髓系驱动基因主导型”,从而指导个体化治疗选择,避免无效的免疫抑制治疗,并对恶性转化高危患者实现早期识别与干预。
二、移植治疗新进展:方案优化升级

阿仑单抗预处理方案:10年OS优异
英国33个中心的大规模回顾性研究(2025 ASH Oral 984)纳入了1999-2024年间所有接受HLA 9-10/10同胞或无关供体移植的SAA和遗传性骨髓衰竭综合征患者,共涵盖数百例移植病例。结果显示:以阿仑单抗为基础的FCC方案(氟达拉滨+环磷酰胺+阿仑单抗)预处理的10年总生存率达85%,10年无GVHD无复发生存率为85%。其中,儿童患者10年OS高达94%。骨髓作为干细胞来源在儿童患者中优势尤为显著(OS 95%vs外周血88%,P=0.01)。年龄越小、使用FCC方案、身体状况越好的患者,预后越佳。
Omidubicel扩增脐带血移植:总生存率94%
对于缺乏HLA匹配供体的难治性SAA患者,一项II期临床研究(2025 ASH Poster 5963)探索了Omidubicel——一种体外烟酰胺扩增脐带血移植方案。研究共纳入18例对IST治疗无效的SAA患者,中位年龄19岁。结果令人振奋:94%的患者实现中性粒细胞恢复(中位8天),89%实现血小板恢复(中位24天),94%达到完全髓系嵌合。无III-IV级急性GVHD或慢性GVHD发生,总生存率达94%。这一方案为无合适供体的高危AA患者提供了可行的替代移植来源。
三、TPO-RA联合IST:一线治疗地位持续巩固
移植虽好,但多数患者仍依靠药物治疗。目前,TPO-RA联合IST已被国内外指南确立为不适合移植SAA患者的一线标准治疗方案。
艾曲泊帕:尽早启动安全可行
一项前瞻性II期研究(2025 ASH Oral 979)评估了在等待确诊检查和启动正式治疗期间,尽早启动低剂量环孢素联合艾曲泊帕方案的安全性与可行性。结果显示:该方案安全可行,无治疗相关严重不良事件,且中性粒细胞计数在hATG治疗前即显著改善。2年复发率(16%vs32%)和高危克隆演进率(3%vs13%)均呈下降趋势,提示尽早干预可能减少骨髓应激造血相关的克隆异常。
海曲泊帕:老年患者疗效更优
北京大学血液病研究所开展的单中心回顾性研究(2025 ASH Poster 1119)纳入了32例年龄≥60岁的SAA或VSAA患者,比较了海曲泊帕联合IST与单纯IST的疗效。结果显示:12个月累积缓解率分别为92.9%和85.7%,完全缓解率分别为35.7%和33.3%。12个月总生存率为83.3%。在Charlson合并症指数更高、粒细胞缺乏更严重的情况下,海曲泊帕联合组仍展现了更优的疗效,且耐受性良好。
2025年专家共识:TPO-RA推荐力度加强
2025年1月,中华医学会血液学分会红细胞疾病学组正式发布《促血小板生成药物治疗再生障碍性贫血专家共识》,对艾曲泊帕、海曲泊帕、罗普司亭等药物的临床应用作出了更明确的推荐,并对SAA、NSAA、TD-NSAA等不同患者类型提供了差异化的治疗路径。共识还特别强调了特殊人群(儿童、孕产妇、老年人、肝功能异常者)的个体化用药策略。
四、新型疗法探索
除了上述成熟的治疗策略,本次ASH年会还公布了多项探索性疗法的研究成果。
IL2RG抗体(REGN7257):首次人体研究展现安全性
REGN7257是一种能阻断IL2RG的单克隆抗体。γ链细胞因子(包括IL2、IL4、IL7、IL9、IL15、IL21)在T细胞发育和激活中起关键作用,阻断其共同受体亚基有望成为抑制致病性T细胞反应的新策略。这项I期、多中心、首次人体研究纳入了17例既往IST治疗难治或复发的SAA患者。结果显示,REGN7257总体耐受性良好。1例IST复发患者在首次给药后即出现血液学反应,且重复给药后反应再次出现。该研究为IL2RG阻断剂在轻症SAA及其他T细胞介导疾病中的进一步探索奠定了基础。
罗特西普+CsA+艾曲泊帕三联疗法:抑制焦亡促进造血
天津医科大学总医院付蓉教授团队的研究(2025 ASH Poster 4976)发现,罗特西普能够通过抑制单核细胞中NF-κB/NLRP3信号轴,实现SAA的多靶点免疫调节。三联疗法显著恢复了SAA患者的造血功能,但停药后仍存在复发问题,提示长期维持治疗的必要性。单细胞RNA测序显示,复发期间单核细胞中焦亡相关基因表达升高。机制层面,罗特西普可显著降低单核细胞焦亡相关基因及促炎细胞因子表达,同时减弱CD8⁺T细胞的炎症因子分泌和细胞毒分子活性,从而破坏致病恶性循环,促进造血恢复。
芦可替尼:降低巨噬细胞焦亡治疗SAA
JAK1/2抑制剂芦可替尼(Ruxolitinib)在SAA治疗中的潜力也受到关注。体外及动物模型实验表明,芦可替尼可通过降低巨噬细胞焦亡水平,改善免疫微环境,并可能通过调控MHC II分子及JAK/STAT通路影响T细胞活化。此外,在仅接受外周血干细胞移植的AA患者中,围移植期加用芦可替尼作为GVHD预防药物,可显著降低II-IV级急性GVHD发生率,并改善患者无GVHD-无失败生存率。
葛林阜院长从机制到临床,AA精准诊疗未来可期
葛林阜院长在授课中强调,2025 ASH大会的研究成果从机制解码、移植优化、药物升级到创新探索,全面推动了AA诊疗的发展。当前AA治疗已形成“移植根治+药物兜底+创新补位”的多元格局,精准化、个体化成为核心趋势。


相关阅读
你是不是还想了解以下问题
- 能治好吗
- 反复发作怎么办
- 需要多少钱
- 什么方法有效
- 多久能治好
- 哪家医院效果好

-
 无假日医院
无假日医院 -
 一对一服务
一对一服务 -
 24小时在线
24小时在线 -
 预约免排队
预约免排队
- 在线咨询
- 预约挂号
- 来院路线
- 返回顶部
济南血液病医院
咨询热线:0531-8695 3333
备案号:鲁ICP备12006985号
工信部链接:http://beian.miit.gov.cn









